Les fondamentaux - Chapitre 2 - Caractéristiques d'une image médicale
E. Durand et E. Blondiaux
Plan du chapitre
- Numérisation, pixels, voxels
- Résolution spatiale
- Bruit
- Contraste
- Images en projection et images en coupes
- Présentation et orientation des images
- Archivage
Une image correspond à la mesure localisée d'un signal physique d'un objet1 dans l'espace, généralement en deux dimensions (2D) ou en trois dimensions (3D). On explore ainsi une partie de l'espace appelée « champ de vue » ou field of view (FOV). Ce champ de vue peut concerner l'organisme entier (imagerie « corps entier ») ou bien être ciblé sur une partie de l'organisme.
1. Le terme d'« objet » est ici utilisé comme en optique où l'on observe l'image d'un objet. En imagerie médicale, l'objet observé est le corps humain ou une partie du corps.
Numérisation, pixels, voxels
Cette image est désormais numérique ou numérisée pour presque toutes les techniques d'imagerie médicale (les films radiologiques à base de sels d'argent, autrefois utilisés, ont désormais disparu ; de même que la photographie numérique a remplacé les anciens films photographiques). On range donc dans des cases d'une mémoire d'ordinateur les mesures des signaux physiques. Comme le nombre de cases est en quantité finie, on ne peut plus conserver une mesure continue de l'information, c'est-à-dire connaître la valeur du signal en chaque point de l'espace ; on est obligé de découper l'objet matériel en petits éléments réguliers appelés voxels (volume elements). Les signaux mesurés dans les voxels sont rangés dans de petits rectangles de l'image en 2D (en petits parallélépipèdes en 3D) qui sont appelés pixels (picture elements). La notion de voxel se rapporte donc à l'élément matériel tandis que la notion de pixel se rapporte à l'image (figure 2.1).
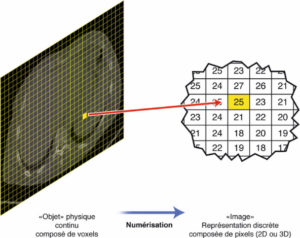
Numérisation d'un objet en image.
Dessin : Emmanuel Durand.
Le signal est donc uniforme au sein d'un pixel dans l'image, alors qu'il ne l'est pas au sein d'un voxel dans l'objet exploré. Ce passage d'un objet réel continu à une image composée de pixels – donc discrète –, appelée conversion analogique-numérique, peut être la source d'artefacts. En particulier, si la taille des pixels est trop grosse, on risque de perdre une partie des détails. Le nombre de pixels dans chacune des dimensions s'appelle la matrice. Par exemple, un champ de vue de 12,8 cm découpé en pixels de 1 mm de côté aura une matrice de 128. Plus la matrice est grande, plus la taille des pixels est petite et plus il est donc théoriquement possible de voir des détails fins (figure 2.2). La matrice est souvent composée de puissances entières de 2, pour des raisons liées aux calculs en traitement de l'image. De même, le nombre de pixels dans les deux dimensions est souvent le même.
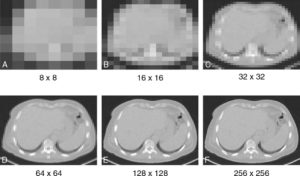
Effet de la matrice (une petite matrice correspond à de gros pixels).
Dessin : Emmanuel Durand.
Résolution spatiale
La résolution spatiale est la capacité à distinguer des structures fines dans l'image. Au sens strict, la résolution spatiale est le nombre de paires de lignes qu'on peut distinguer dans une image par unité de longueur. Par exemple, si on distingue deux points séparés de 2 mm, mais qu'on ne distingue plus des points plus rapprochés, on dira que la résolution spatiale est de 0,5 mm–1. Par abus de langage, on parle le plus souvent d'une résolution de 2 mm dans ce cas.
La résolution est bien sûr conditionnée par la taille des pixels. Par exemple, si la taille d'un pixel est de 2 mm, la résolution la plus fine qu'on puisse espérer voir est de 0,25 mm− 1, c'est-à-dire des structures espacées de 4 mm (figure 2.3).
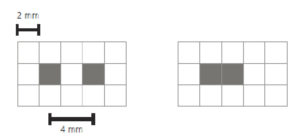
On ne peut distinguer deux pixels noirs que s'ils sont espacés d'un pixel blanc (A) ; sur la figure de droite, on ne distingue qu'une seule structure (B). La résolution spatiale la plus fine permise est donc 1/(2 pixels).
Dessin : Emmanuel Durand.
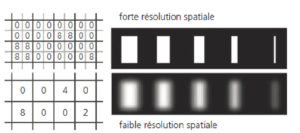
Toutefois, s'il n'est pas possible de voir une résolution plus fine que ce que permet la taille des pixels, cette dernière ne fait pas tout. En effet, la qualité de l'instrument d'imagerie a un rôle majeur et si la résolution intrinsèque de l'appareil est mauvaise, découper l'image en pixels très fins ne résoudra rien (figure 2.4).
La taille des pixels peut limiter la résolution spatiale, mais la résolution spatiale n'est pas la taille des pixels : elle dépend aussi de la qualité de l'appareil d'imagerie !

La taille des pixels est la même dans les deux figures (A, B) ; pourtant, la figure de gauche a une bien meilleure résolution (A).
Dessin : Emmanuel Durand.
Lorsque des structures sont plus petites que ce que permet de voir la résolution spatiale, elles peuvent :
- ne pas être visibles ;
- être visibles mais floues (figure 2.4) ;
- être vues mais avec un niveau de signal incorrect, par moyennage avec les structures qui les entourent ; on parle alors d'effet de volume partiel (figure 2.5).
Effet de volume partiel.
En haut, la résolution spatiale est suffisante pour mesurer le signal avec une intensité correcte ; en bas, une résolution spatiale trop faible entraîne en moyennage des structures les plus petites avec leur entourage (ici, les structures sont sur un fond à signal nul : le niveau de signal est donc sous-estimé) : il s'agit d'un effet de volume partiel.
Dessin : Emmanuel Durand.
Bruit
Dans le domaine du traitement du signal et de l'image, le bruit correspond à un phénomène aléatoire qui se surajoute à l'image idéale. Probablement la meilleure approche pour comprendre le bruit est de comprendre que si l'on acquiert plusieurs fois l'image d'un même objet, immobile et inchangé, on n'observera pas exactement le même résultat : la différence est liée au bruit. De la même manière, en lançant plusieurs fois un dé, on n'obtient pas le même résultat : c'est aléatoire (figure 2.6).
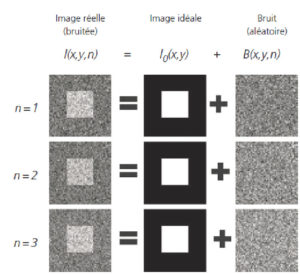
Si l'on répète l'acquisition d'une image à différents temps (n = 1, n = 2, etc.), on obtient des images différentes d'une fois à l'autre.
Dessin : Emmanuel Durand.
La partie constante est l'image idéale, la partie variable est le bruit.
Comme tout phénomène aléatoire, le bruit est caractérisé par son écart type (racine carrée de la variance), qu'on note σ.
Pour quantifier le niveau de bruit, on compare généralement l'intensité du signal avec l'écart-type du bruit pour déterminer le rapport signal sur bruit (RSB) :
où S est l'intensité du signal. Le bruit dans l'image peut gêner l'interprétation et, à l'extrême, rendre les images complètement illisibles. La présence de bruit va également détériorer la résolution spatiale puisqu'il peut être impossible de distinguer des structures trop petites dans une image très bruitée (figure 2.7).

Différents niveaux de rapports signal sur bruit (RSB).
Un RSB de 1 permet encore de distinguer les plus grosses structures mais plus les structures les plus fines.
Dessin : Emmanuel Durand.
Contraste
Un diagnostic est généralement fait en discernant le signal anormal d'une lésion au sein d'un organe normal. C'est donc le contraste entre les deux qui permet le diagnostic. Le signal de l'organe normal est parfois appelé « bruit de fond » en français. Ce terme n'est pas très heureux car il fait référence au bruit (aléatoire) alors qu'il ne s'agit pas de bruit ici. Le terme anglais background est plus adapté.
Si l'on note S1 le signal de la lésion et S2 le signal de fond, le contraste est traditionnellement défini comme : C = | S1 - S2 | / | S1 + S2 |
Un signal de 6 sur un fond de 2 donne donc un contraste de 0,5. Toutefois, sur une image numérique, il est aisé de changer le contraste à volonté. Dans l'exemple précédent, si l'on soustrait la valeur 4 à l'image, les deux valeurs précédentes deviennent respectivement + 2 et − 2 avec un contraste qui devient infini. Plus intéressant est donc de considérer le rapport contraste sur bruit (RCB) : RCB = C = | S1 - S2 | / σ
Images en projection et images en coupes
L'objet étudié est fondamentalement tridimensionnel. Certaines modalités d'imagerie fournissent une image tridimensionnelle (imagerie en coupes) ; d'autres ne permettent d'obtenir qu'une image 2D (tableau 2.1). Il s'agit donc d'une projection de l'objet initial, comme une ombre chinoise (figure 2.8). On perd alors l'information de profondeur, la quantification devient difficile et les superpositions peuvent gêner l'interprétation.
Tableau 2.1
Types et mécanismes des différentes modalités d'imagerie
|
Type |
Mécanisme |
Modalité |
2D/3D |
|
Morphologique |
Absorption des rayons X |
Radiographie Angiographie numérisée |
Projection 2D |
|
Angiographie rotationnelle TDM (scanner) |
3D |
||
|
Réflexion des ultrasons |
Échographie |
Coupes 2D |
|
|
Échographie 3D |
3D |
||
|
Mixte |
Échos de l'aimantation des noyaux |
IRM |
3D |
|
Fonctionnelle |
Émission de photons gamma |
Scintigraphie |
Projection 2D |
|
Tomoscintigraphie
|
3D |
||
|
Émission de positons |
TEP |
3D |
Présentation et orientation des images
Par convention, les images sont présentées de la même façon au sein d'une modalité, qu'elle soit en projection ou en coupes (figure 2.8) :
• en projection de face ou en coupe coronale (ou frontale), la droite du patient est présentée à gauche de l'écran : comme si on regardait simplement le patient de face ;
• sur une vue axiale (ou transverse), la droite du patient est toujours située à gauche de l'écran : comme si on regardait le patient – allongé sur le dos – depuis ses pieds ;
• sur une vue sagittale ou de profil, l'image est présentée avec la partie antérieure du patient à gauche de l'écran, comme si on regardait le patient de profil gauche (à l'exception des images d'échographie sur lesquelles le pôle crânial du patient est présenté à gauche de l'écran)
• les images de scintigraphie planaire (projections) sont toujours représentées comme si l'observateur avait le point de vue de la caméra (voir chapitre 5).
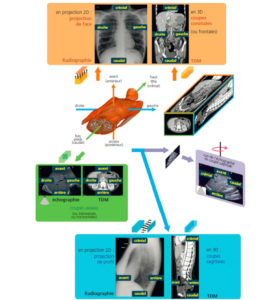
Orientation conventionnelle des images : coupes axiales, coronales et sagittales de TDM ; projections de face et profil en radiographie.
L'orientation est normalisée pour ces différentes images. Elle est la même en IRM et en tomoscintigraphie. Les coupes sagittales d'échographie sont représentées différemment, le pôle crânial étant placé à gauche de l'écran.
Dessin : Emmanuel Durand.
Archivage
Les images médicales sont enregistrées sous un format de stockage et d'échange appelé digital imaging communication in medicine (DICOM) qui contient, outre l'image elle-même, des métadonnées la caractérisant (identité du patient, date et heure d'acquisition, type d'appareil, paramètres d'acquisition détaillés, etc.). Dans les établissements de santé, les images sont désormais archivées dans un système en réseau appelé Picture Archiving and Communication System (PACS), habituellement consultable également par les correspondants.
 |
Chapitre suivant |
 |
Retour au sommaire |
Les fondamentaux - Chapitre 1 - Histoire de l'imagerie médicale
F. Brunotte et P. Devred
L'histoire de l'imagerie médicale a à peine plus d'une centaine d'années (liste 1.1). Elle a comporté des va-et-vient permanents entre la physique, l'anatomie, la biologie, la chimie et les spécialités médicales qui soulignent son caractère profondément pluridisciplinaire. La liste des prix Nobel qui ont influencé cette spécialité est là pour en témoigner (liste 1.2).
Liste 1.1 - Sélection de quelques dates essentielles de l'évolution de l'imagerie
- 1895 - W.C. Röntgen réalise la première image du squelette de la main de son épouse avec les rayons X
- 1897 - Premier laboratoire de radiologie créé par A. Béclère à l'hôpital Tenon (Paris)
- 1909 - Création par A. Béclère de la Société de radiologie médicale de Paris, devenue depuis Société française de radiologie en se séparant des physiciens : « Nul ne peut devenir un bon radiologiste sans être avant tout un bon clinicien »
- 1914 - Début de l'utilisation des produits de contraste opaques aux rayons X à base de bismuth, potasse, baryum pour le tube digestif et de sels d'argent pour les voies urinaires
- 1914–1918 - La radiologie contribue à la prise en charge des blessés au plus près des combats (voiturettes équipées à l'initiative de Marie Curie)
- 1918 - W.E. Dandy réalise la première ventriculographie gazeuse par injection directe d'air dans les ventricules cérébraux
- 1920 - Début de l'utilisation du thorium (Thorotrast) comme produit de contraste qui se révélera plus tard être responsable de cancers hépatiques du fait de la radioactivité alpha du thorium
- 1921 - A. Bocage dépose le brevet du premier tomographe aux rayons X
- 1923 - E.D. Osborne utilise l'iodure de sodium pour opacifier les voies urinaires
- 1923 - G.C. de Hevesy introduit le concept de traceur en montrant l'intérêt du plomb 210 pour suivre le devenir du plomb dans les plantes
- 1926 - H.L. Blumgart s'injecte du bismuth 214 dans une veine du bras et mesure la vitesse sanguine
- 1927 - Introduction des dérivés iodés de la pyridone comme contraste pour l'urographie par M. Swick
- 1928 - A.E. Moniz, à Lisbonne, publie les premières artériographies cérébrales à l'iodure de sodium par ponction carotidienne directe
- 1929 - W. Forssmann s'introduit un cathéter dans une veine du bras et le pousse jusqu'au cœur et ouvre ainsi la voie de la radiologie vasculaire
- 1932 - O. Chievitz et G.C. de Hevesy suivent le métabolisme du phosphore à l'aide du phosphore 32 chez le rat
- 1936 - Inauguration à Hambourg du monument en l'honneur des pionniers de la radiologie victimes de cancers et de leucémies radio-induits : « à ceux qui ont sacrifié leur vie dans la lutte contre les maladies et ont été les pionniers d'une application féconde des rayons de Röntgen… immortelle est la gloire de ces morts »
- 1937 - J.H. Lawrence utilise le phosphore 32 pour tenter de traiter une leucémie
- 1946 - S.M. Seidlin traite des métastases d'un cancer thyroïdien par l'iode 131 (131I)
- 1950 - B. Cassen introduit le premier dispositif d'imagerie par scintigraphie, le scanner rectilinéaire
- 1952 - J.J. Wild, L. Leksell et I. Edler utilisent pour la première fois les ultrasons pour l'étude du cœur. S.I. Seldinger développe l'abord percutané des artères périphériques pour la radiologie vasculaire
- 1957 - Invention de la gamma-caméra par H.O. Anger à Berkeley
- 1958 - L'Anglais I. Donald réalise la première échographie de l'utérus
- 1958 - W.D. Tucker et M.W. Greene décrivent le générateur de 99mTc au Brookhaven National Laboratory
- 1960 - Premières embolisations de malformations vasculaires en neuroradiologie par S. Wallace, R. Djindjian et J.J. Merland
- 1962 - Le Commissariat à l'énergie atomique (CEA) en France est le deuxième client du générateur de technétium après Chicago
- 1963 - D.E. Kuhl introduit la tomographie d'émission monophotonique
- 1972 - L'Anglais G.N. Hounsfield et l'Américain A.M. Cormack inventent le scanner X
- 1971–1973 - Les Américains R. Damadian et P.C. Lauterbur réalisent les premières images d'IRM
- 1973 - M.E. Phelps et E.J. Hoffman introduisent le premier appareil de tomographie par émission de positons (TEP)
- 1975 - Début de la diffusion de l'échographie médicale. A. Gruentzig crée le cathéter de dilatation vasculaire par ballonnet
- 1976 - Premier scanner X installé en France (Marseille)
- 1976 - A. Alavi injecte du fluorodésoxyglucose marqué au fluor 18 (18F-FDG) pour la première fois à un homme
- 1980 - Commercialisation des premières IRM
- 1983 - Premiers essais cliniques du DTPA-Gd comme agent de contraste en IRM
- 1985 - Premières endoprothèses vasculaires (stent)
- 2000 - T. Beyer et D.W. Townsend introduisent l'imagerie hybride couplant TEP et scanner X
- 2010 - Introduction de l'imagerie couplant TEP et IRM
- 2017 - Premières applications de l'intelligence artificielle susceptibles de se comparer à l'interprétation d'un spécialiste pour la détection d'anomalies sur des examens d'imagerie médicale
Liste 1.2 - Prix Nobel en lien avec l'imagerie
- 1901 - W.C. Röntgen (Allemagne), physique, en reconnaissance des services extraordinaires qu'il a rendus en découvrant les remarquables rayons qui ont été nommés par la suite en son honneur
- 1903 - A.H. Becquerel, P. Curie, M. Curie (France), physique, en témoignage des services extraordinaires rendus par la découverte de la radioactivité spontanée et les phénomènes radiatifs
- 1911 - M. Curie (France), chimie, en reconnaissance des services pour l'avancement de la chimie par la découverte de nouveaux éléments : le radium (Ra) et le polonium (Po), par l'étude de leur nature et de leurs composés
- 1935 - F. Joliot et I. Joliot-Curie (France), chimie en reconnaissance de la synthèse de nouveaux éléments radioactifs
- 1943 - G.C. de Hevesy (Suède), chimie, pour son travail dans le domaine des traceurs radioactifs
- 1944 - I.I. Rabi (États-Unis), physique pour sa méthode de résonance servant à enregistrer les propriétés magnétiques du noyau atomique
- 1946 - H.J. Muller (États-Unis), physiologie et médecine, pour ses recherches sur les mutations induites par les rayons X
- 1949 - A.E. Moniz (Portugal), physiologie et médecine, pour le développement de la leucotomie préfrontale (lobotomie) appliquée au traitement de certaines psychoses et troubles mentaux (inventeur de l'artériographie cérébrale)
- 1952 - F. Bloch et E.M. Purcell (États-Unis), physique pour leur développement de nouvelles méthodes de mesures magnétiques nucléaires fines et les découvertes qui en ont découlé
- 1956 - A.F. Cournand (États-Unis), W. Forssmann (Allemagne), D.W. Richards (États-Unis), physiologie et médecine pour leur découverte concernant le cathétérisme cardiaque et les changements pathologiques dans le système circulatoire
- 1979 - A.M.Cormack (États-Unis), G.N. Hounsfield (Royaume-Uni), physiologie et médecine pour la production d'images tomographiques en imagerie par rayons X
- 1991 - R.R. Ernst (Suisse), chimie pour ses contributions au développement de la méthodologie de la spectroscopie de la résonance magnétique nucléaire à haute définition
- 1992 - G. Charpak (France), physique pour son invention et le développement de détecteurs de particules, en particulier la chambre « multifils »
- 2003 - P.C. Lauterbur (États-Unis), P. Mansfield (Royaume-Uni), physiologie et médecine pour leurs découvertes concernant l'imagerie par résonance magnétique
Si les tout-débuts de son développement ont mis en danger médecins et patients en raison de la nocivité des rayons X, de certains produits de contraste comme le Thorotrast (produit de contraste à base de thorium, composé radioactif utilisé dans les années 1930–1940, qui s'est révélé par la suite cancérigène) ou de certaines techniques, l'imagerie permet aujourd'hui une approche morphologique et fonctionnelle remarquable du corps humain, le plus souvent de manière simple et sans risque.
Ces progrès ont changé l'approche des maladies. Prenons l'exemple du diagnostic des tumeurs cérébrales. L'arrivée des rayons X permit seulement de les mettre en évidence par l'intermédiaire de leur retentissement osseux ou des calcifications qu'elles contenaient. L'idée d'utiliser les agents de contraste apparut donc rapidement, d'abord par un contraste négatif grâce à l'injection d'air dans les espaces liquidiens du cerveau (douloureux), puis par injection de contraste dans les carotides sous anesthésie générale après dénudation chirurgicale de la carotide. En dépit de ses progrès, l'artériographie restait agressive et, à partir de 1950, la médecine nucléaire occupa le terrain de l'imagerie sans danger pour le patient avec la fluorescéine marquée à l'iode, le mercure -203 et surtout l'acide diéthylène triamine penta acétique (DTPA) marqué au technétium -99m (99mTc) qui régna comme la méthode de référence jusqu'au développement explosif du scanner (ou tomodensitométrie [TDM]) à partir de 1971. Depuis la fin des années 1980, l'imagerie par résonance magnétique (IRM) avec le DTPA-gadolinium (Gd) est devenue la méthode de référence de l'imagerie des tumeurs cérébrales.
Ainsi, l'imagerie n'est pas figée et des techniques qui paraissaient incontournables comme l'urographie intraveineuse, les opacifications digestives, ou certaines scintigraphies ont presque disparu, remplacées par l'échographie, la TDM, l'IRM et de nouveaux radiopharmaceutiques en médecine nucléaire.
Chaque technique a ses domaines d'excellence : les ultrasons sont irremplaçables aujourd'hui dans le suivi des grossesses ou en cardiologie ; la TDM et l'IRM ont chacune leur place en neuroradiologie et dans l'ensemble de l'imagerie ; la médecine nucléaire s'est affirmée pour l'approche moléculaire des maladies et de leur traitement, etc.
 |
Chapitre suivant |
 |
Retour au sommaire |
Les fondamentaux - Terminologie en imagerie
Une structure s'analyse en fonction de son signal absolu ou relatif (par rapport aux organes ou tissus adjacents).
Tableau 1 - Résumé des principaux termes descriptifs du signal en imagerie
|
Radiographie |
TDM |
Echographie |
IRM |
médecine nucléaire |
|
|
Blanc |
opacité |
hyperdense |
hyperéchogène |
hypersignal |
hyperfixant |
|
Gris |
intermédiaire |
isodense |
isoéchogène |
isosignal |
isofixant |
|
Noir |
clarté |
hypodense |
anéchogène |
hyposignal |
hypofixant |
Radiographie
- Opacité = zone de forte densité (blanche)
- Clarté = zone de moindre densité (sombre ou noire)
- Une structure dense (Z élevé), comme l'os, atténue (absorbe) beaucoup les RX c'est à dire est « radio-opaque » (blanche)
- Une structure aérique (Z faible), comme les poumons, atténue peu les RX c'est à dire apparaît comme une « hyper clarté » (sombre ou noire)
- Structure intermédiaire : tissus mous peu contrastés nécessitant parfois l'utilisation de produits de contraste à Z élevé : baryum (Z = 56) ou iode (Z = 53)
Tomodensitométrie
Le principe est le même que pour la radiographie mais on utilise une terminologie un peu différente :
- Hypodense : par exemple la valeur – 1000 UH attribuée à l'air (noir)
- Isodense : la valeur 0 UH est attribuée à l'eau (intermédiaire) ou se dit d'une structure de même densité que le parenchyme normal
- Hyperdense : par exemple la valeur + 1000 UH attribuée à l'os compact (blanc)
Échographie
- Anéchogène (noire) : liquide homogène, absence d'interfaces donc absence d'écho
- Hypoéchogène (intermédiaire)
- Hyperéchogène (blanche)
- Cône d'ombre postérieur : vide d'échos en arrière d'une structure absorbante qui est hyperéchogène
- Renforcement postérieur des ultrasons : renforcement de l'intensité du faisceau d'ultrasons en arrière d'une structure non absorbante qui est anéchogène
- Echos de réverbération ou image en queue de comète : réflexions multiples sur deux interfaces très réfléchissantes
IRM
- Hypersignal (ou hyperintense) : blanc
- Hyposignal (ou hypointense) : noir
- Isosignal (ou isointense) : de signal intermédiaire ou se dit d'une structure de même signal que le parenchyme normal
Médecine nucléaire
- Hyperfixation (ou hypermétabolisme) : signal plus intense lié à une concentration plus forte du radiopharmaceutique injecté, généralement lié à un métabolisme plus intense
- Hypofixation (ou hypométabolisme) : signal moins intense.
Radioanatomie
Noeuds lymphatiques (nomenclature internationale) : lieu de prolifération et de différenciation des cellules immunitaires. Le terme « ganglions lymphatiques » est utilisé dans le langage courant et en de rares occasions dans cet ouvrage. Une technique de repérage des noeuds lymphatiques a une appellation consacrée : « technique du ganglion sentinelle ».
 |
Chapitre suivant |
 |
Retour au sommaire |
Les fondamentaux - Préface
La radiologie et imagerie médicale ainsi que la médecine nucléaire sont des spécialités peu connues des étudiants, vues souvent comme complexes et techniques. Leur premier contact se fait souvent au cours des examens de sélection des premières années avec des exercices de doses, d'activité de traceur, de fixation, de décroissance de radioactivité.
Il est vrai qu'un minimum de connaissances est nécessaire pour appréhender les possibilités offertes par les examens d'imagerie. D'un côté, la radio-anatomie exige de l'étudiant que vous êtes de ré-apprendre l'anatomie du corps humain d'une manière différente, dans des plans de coupes transverses, sagittales, coronales, voire obliques ou double-obliques alors que l'apprentissage de l'anatomie demande en soi un investissement conséquent. D'un autre côté, les examens de médecine nucléaire reposent sur des processus physiopathologiques nombreux et variés qui expliquent la biodistribution des médicaments radiopharmaceutiques utilisés. De plus, les examens proposés permettent maintenant de superposer à l'anatomie des informations de fonctions, de métabolisme, de perfusion, de viabilité, de nécrose… venant amplifier les renseignements fournis aux demandeurs.
Et pourtant, tous les jours, quelle que soit votre discipline de demain, vous serez amenés à demander des examens, à les comprendre, à les expliquer à vos patients. Le radiologue et le médecin nucléaire sont des médecins qui seront vos correspondants dans un travail d'équipe permettant des soins de qualité car coordonnés et adaptés aux patients en fonction de la demande de dépistage, de diagnostic, de suivi ou de traitement par radiologie interventionnelle ou par radiothérapie interne vectorisée. L'imagerie est présente pour l'exploration de toutes les pathologies ou presque, quel que soit l'âge de la Vie. Nos disciplines sont transversales dans l'enseignement des EDN et vous devez connaitre les indications, contre-indications, modalités de réalisation, résultats attendus, les conduites à tenir pour les principales pathologies.
La radiologie et la médecine nucléaire ont fait des progrès considérables ces dernières années rendant leurs indications plus complexes et plus nombreuses. Vous trouverez dans ce livre des éléments de base pour comprendre comment sont réalisés les examens afin de pouvoir les expliquer aux patients, obtenir leur accord, connaitre les indications, les contre-indications et les conduites à tenir selon les résultats obtenus. Votre responsabilité sera engagée dès que vous demanderez un examen mais cette responsabilité sera partagée avec le radiologue ou le médecin nucléaire contrairement aux pharmaciens ou biologistes qui exécuteront votre prescription. Sachez travailler main dans la main avec nous pour offrir à nos patients le meilleur des soins. Trop de médecins demandent l'examen radiologique avant de réaliser un examen clinique : cette tendance doit être combattue car à une question vague, la réponse apportée par l'imagerie restera vague. Si la question est ciblée par votre interrogatoire et votre examen clinique, l'examen radiologique ou de médecine nucléaire permettra de vous apporter une réponse plus adaptée.
Dans ce livre vous trouverez toutes les informations utiles pour vos examens. Nous vous souhaitons un bon apprentissage de l'imagerie médicale et vous invitons à ne pas hésiter à compléter vos connaissances par un ou plusieurs stages dans nos services pour mieux vous approprier ces examens. N'hésitez pas à nous contacter pour comprendre les possibilités des examens et traitements proposés, afin de choisir celui qui sera le plus adéquat dans le contexte clinique donnée, nous sommes des médecins et soignants à votre disposition.
Jean-Paul Beregi Pr , Damien Huglo Pr et Michel Montaudon Pr
 |
Chapitre suivant |
 |
Retour au sommaire |
Les fondamentaux - Les auteurs
Coordinateurs
- Éléonore Blondiaux, PU-PH, service d'imagerie, Hôpital Armand Trousseau, AP-HP ; Sorbonne Université, Paris
- Emmanuel Duran, PU-PH, chef de service, service de biophysique et médecine nucléaire, Hôpitaux Universitaires Paris Sud, Hôpital Bicêtre, AP-HP, Le Kremlin-Bicêtre ; coordonnateur national du DES de médecine nucléaire, Université Paris Saclay
- Michel Montaudo, PU-PH, laboratoire d'anatomie, Université de Bordeaux, Bordeaux
Auteurs
- Ronan Abgra, PU-PH, service de médecine nucléaire, Hôpital Augustin Morvan, CHRU de Brest, Brest
- Lionel Arriv, PU-PH, service d'imagerie médicale, Hôpital Saint-Antoine, AP-HP ; Sorbonne Université, Paris
- Fayçal Ben Bouallègue†, MCU-PH, médecine nucléaire, Hôpital Lapeyronie, CHU de Montpellier, Montpellier
- Jean-Paul Beregi,PU-PH, service de radiologie, CHU Caremeau, Nîmes
- Florent Besson, MCU-PH, service de biophysique et médecine nucléaire, Hôpitaux Universitaires Paris Sud, Le Kremlin-Bicêtre ; Université Paris Saclay
- Guillaume Bierry, PU-PH, service de radiologie 2, Hôpitaux Universitaires de Strasbourg, Strasbourg
- Cyrille Blondet, MCU-PH, service biophysique et médecine nucléaire, Hôpitaux Universitaires de Strasbourg, Strasbourg
- Alain Blum, PU-PH, service d'imagerie Guilloz, Hôpital Central, CHU de Nancy, Nancy
- Gérald Bonardel, professeur agrégé du Val-de-Grâce, service de médecine nucléaire, Centre, cardiologique du Nord, Saint-Denis
- François Brunotte, professeur émérite, biophysique et médecine nucléaire, Dijon
- Florent Cachin, PU-PH, service de médecine nucléaire, Centre Jean Perrin de lutte contre le cancer, Clermont-Ferrand
- Sophie Cahen-Riehm, PH, service d'imagerie 1, Hôpital de Hautepierre, CHU de Strasbourg, Strasbourg
- Pascal Chabrot, PU-PH, CHU de Clermont-Ferrand, Radiologie Montpied, Institut Pascal, UMR 6602 CNRS SIGMA UCA, Clermont-Ferrand
- Agathe Chammas, PH, service d'imagerie 2, CHU de Hautepierre, Strasbourg
- Jean-François Chateil, PU-PH, chef de service, service d'imagerie anténatale, de l'enfant et de la femme, Université de Bordeaux, CHU Pellegrin, Bordeaux
- Olivier Chevallier, CCA, département de radiologie diagnostique et thérapeutique, Hôpital François Mitterrand, CHU de Dijon, Dijon
- Alexandre Cochet, PU-PH, chef de service, service de médecine nucléaire, Université de Bourgogne, UFR des Sciences de santé, service de spectroscopie RMN et IRM cardiaque Centre Georges-François Leclerc et CHU de Dijon, Dijon,
- Emmanuel Deshayes, MCU-PH, service de médecine nucléaire, Institut du Cancer de Montpellier ; Faculté de médecine Montpellier-Nîmes, Université de Montpellier
- Jean-Yves Devaux, professeur honoraire de biophysique et de médecine nucléaire, Paris
- Philippe Devred, PU-PH, service d'imagerie pédiatrique et prénatale, Hôpital de la Timone Enfant, AP-HM ; Université Aix-Marseille, Marseille
- Gilbert Ferretti, PU-PH, clinique universitaire de radiologie et imagerie médicale, CHU de Grenoble Alpes, Grenoble
- Laure Fournier, PU-PH, service de neuroradiologie, Hôpital européen Georges Pompidou, AP-HP ; Université de Paris Cité, Paris
- Damien Galanaud, PU-PH, Hôpital de la Pitié-Salpêtrière, AP-HP ; Sorbonne Université, Paris
- Pedro Augusto Gondim Teixeira, PU-PH, service de radiologie Guilloz, Hôpital Central, CHU de Nancy, Nancy
- Gilles Grimon, MCU-PH, service de biophysique et médecine nucléaire, Hôpital Bicêtre, AP-HP, Le Kremlin-Bicêtre ; Université Paris Saclay, Faculté de médecine
- Vincent Hazebroucq, MD PhD, MCU-PH détaché en tant que médecin responsable de programmes d'inspection et d'audit à l'ARS Île-de-France
- Damien Huglo, PU-PH, chef de service, service de médecine nucléaire, CHRU de Lille, Lille
- Olivier Humbert, PU-PH, Faculté de médecine de Nice Sophia Antipolis, Nice
- Isabelle Keller-Petrot, PH, service de médecine nucléaire pédiatrique, Hôpital Armand Trousseau, AP-HP ; Sorbonne Université, Paris
- Dris Kharroubi, AHU, service de médecine nucléaire, Groupe hospitalier Pitié-Salpêtrière, AP-HP, Paris
- Stéphane Kremer, PU-PH, service d'imagerie 2, Hôpital de Hautepierre, CHU de Strasbourg, Strasbourg
- Claire de Labriolle-Vaylet, MCU-PH honoraire, service de médecine nucléaire, Hôpital Armand-Trousseau, AP-HP ; Sorbonne Université, Paris
- Alain Lalande, MCU-PH, service de spectroscopie, Hôpital François Mitterrand, CHU de Dijon ; LE2I Faculté de médecine, Université de Bourgogne Franche-Comté, Dijon
- Vincent Lebon, PU-PH, service de médecine nucléaire Frédéric Joliot, Orsay ; UFR de médecine, Université Paris-Saclay, UMR BioMaps, CEA-SHFJ, Orsay
- Florence Le Jeune, PU-PH, service de médecine nucléaire, Centre Eugène Marquis, CHU de Rennes
- Pierre-Yves Le Roux, PU-PH, service de biophysique et médecine nucléaire, CHRU de Brest, Brest
- Romaric Loffroy, PU-PH, département de radiologie diagnostique et thérapeutique, Hôpital François-Mitterrand, CHU de Dijon, Dijon
- Benjamin Longère, PH, service de radiologie et imagerie cardiovasculaire, Institut Cœur-Poumon, CHRU de Lille, Lille
- Olivier Lucidarme, PU-PH, chef de service, service de radiologie polyvalente et oncologique, Groupe hospitalier Pitié-Salpêtrière, AP-HP ; Sorbonne Université, Paris
- Charlotte Lussey-Lepoutre, PU-PH, responsable de l'unité fonctionnelle de radiothérapie interne vectorisée, service de médecine nucléaire, Hôpital Pitié-Salpêtrière, AP-HP, Paris ; Sorbonne Université
- Damien Mandry, PU-PH, service de radiologie, Hôpitaux de Brabois, CHRU de Nancy, Vandœuvre-lès-Nancy ; Université de Lorraine, Faculté de médecine, Nancy
- Denis Mariano-Goulart, PU-PH, chef de service médecine nucléaire, Hôpital Lapeyronie, CHU de Montpellier, Montpellier
- Fatima-Zohra Mokrane, PU-PH, service de radiologie, Hôpital Rangueil, CHU de Toulouse ; Unité INSERM I2MC-équipe 13-Toulouse
- Sébastien Molière, PH, service d'imagerie 1, Hôpital de Hautepierre, CHU de Strasbourg, Strasbourg
- Mickaël Ohana, PU-PH, service d'imagerie diagnostique cardiovasculaire et thoracique, Nouvel Hôpital Civil, Strasbourg
- Frédéric Patat, ingénieur, PU-PH, service échographie Doppler, CHRU de Tours ; CIC IT 1415 Ultrasons et Radiopharmaceutiques, Tours
- François Pontana, PU-PH, chef de service, service radiologie et imagerie cardiovasculaire, Institut Cœur-Poumon, CHRU de Lille, Lille
- Alban Redheuil, PU-PH, département d'imagerie cardiovasculaire et de radiologie interventionnelle et thoracique, Institut de cardiologie, Groupe hospitalier La Pitié Salpêtrière ; Sorbonne Université, Faculté de médecine ; ICAN (Institute of Cardiometabolism and Nutrition) ; LIB Biomedical Imaging Laboratory, Cardiovascular Research Team (INSERM/CNRS/UPMC), Paris
- Raphaële Renard-Penna, PU-PH, Hôpitaux Tenon-Pitié Salpêtrière, AP-HP ; Sorbonne Université, Paris
- Maxime Ronot, PU-PH, service de radiologie, Hôpitaux Universitaires Paris Nord-Val-de-Seine, Hôpital Beaujon, Clichy
- Edmond Rust, médecin nucléaire, médecine nucléaire, Clinique du Diaconat, Mulhouse
- David Taïeb, PU-PH, service de médecine nucléaire, Hôpital de la Timone, AP-HM, Marseille
- Isabelle Thomassin-Naggara, PU-PH, département de radiologie, Hôpital Tenon, AP-HP ; Sorbonne Université, Paris
- Thomas Tourdias, PU-PH, service de neuroimagerie diagnostique et thérapeutique, CHU de Bordeaux
- Paul Michael Walker, MCU-PH, imagerie médicale application clinique, département Vision, LE2I, UMR CNRS 6306, Faculté de médecine, Université de Bourgogne-Franche-Comté, Dijon
Contributeurs de la première édition
- Louis Boyer, PU-PH, pôle radiologie et imagerie médicale, Hôpital Gabriel Montpied, CHU de Clermont-Ferrand, Clermont-Ferrand
- Sophie Chagnon-Lhespitaou†, PU-PH, service de radiologie, Hôpital Ambroise Paré, UFR Paris-Île de, France Ouest
- Philippe Chaumet-Riffaud, PU-PH, service de biophysique et de médecine nucléaire, Hôpitaux Universitaires Paris Sud, Le Kremlin-Bicêtre ; Université Paris Saclay
- Anne Cotten, PU-PH, service de radiologie et imagerie musculosquelettique, CCIAL, CHRU de Lille, Lille
- Olivier Couturier, PU-PH, chef de Service, service de médecine nucléaire et biophysique CHU d'Angers, Angers
- Valérie Croisé-Laurent, PU-PH, Radiologie Brabois adultes, Hôpitaux de Brabois, CHRU de Nancy, Vandœuvre-lès-Nancy
- Jean-Nicolas Dacher, PU-PH, chef de service, service d'imagerie médicale, CHU Charles Nicolle, Rouen
- Jacques Darcourt, PU-PH, Biophysique et médecine nucléaire, Faculté de médecine, Université Côte d'Azur, Nice
- Hubert Ducou le Pointe, PU-PH, chef de service, service de radiologie pédiatrique, Hôpital Armand-Trousseau, AP-HP ; Université Pierre et Marie Curie, Paris
- Olivier Ernst, PU-PH, chef de service, service d'imagerie digestive et endocrinienne, Hôpital Huriez, CHRU de Lille, Lille
- Astrid Girma, médecin nucléaire, médecine nucléaire, Hôpital Foch, Suresnes
- Boris Guiu, PU-PH, chef de service, département de radiologie diagnostique et interventionnelle, Hôpital Saint-Éloi, CHU de Montpellier, Montpellier
- Olivier Hauger, PU-PH, responsable unité d'imagerie ostéo-articulaire, service d'imagerie diagnostique et thérapeutique de l'adulte, Hôpital Pellegrin, CHU de Bordeaux, Bordeaux
- Olivier Hélénon, PU-PH, chef de service, service radiologie adultes, Hôpital Necker-Enfants malades, AP-HP, Paris
- Elif Hindie, PU-PH, service de médecine nucléaire Sud et Pellegrin, CHU de Bordeaux, Pessac
- Emmanuel Itti, PU-PH, chef de service, service de médecine nucléaire, CHU Henri Mondor, AP-HP ; Université Paris-Est Créteil, Créteil
- Bruno Kastler, PU-PH, service de radiologie adultes, Hôpital Necker-Enfants malades, AP-HP, Paris
- Alain Luciani, PU-PH, service d'imagerie médicale, Faculté de médecine de Créteil, Université Paris Est Créteil, INSERM U955 Équipe 18, CHU Henri Mondor, Créteil
- Xavier Marchandise, professeur honoraire de biophysique et médecine nucléaire, service de médecine nucléaire Imanord, Villeneuve d'Ascq
- Pierre-Yves Marie, PU-PH, service de médecine nucléaire, Hôpitaux de Brabois, CHRU de Nancy, Vandœuvre-lès-Nancy
- Guillaume Marzolf, CCA, service d'imagerie 2, Hôpital de Hautepierre, CHU de Strasbourg, Strasbourg
- Nicolas Menjot de Champfleu, PU-PH, service de neuroradiologie, Hôpital Gui de Chauliac, CHU de Montpellier, Montpellier
- Guy Mouli, PU-PH, service de radiologie adultes, Hôpital de la Timone, AP-HM, Marseille
- Olivier Mundle, PU-PH honoraire, service de médecine nucléaire, Hôpital de la Timone, AP-HM, Marseille
- Pierre Olivie, PU-PH, service de médecine nucléaire, Hôpitaux de Brabois, CHU de Nancy, Vandœuvre-lès-Nancy
- Catherine Oppenhei, PU-PH, service d'imagerie morphologique et fonctionnelle, Hôpital Sainte-Anne, Paris
- Philippe Ota, PU-PH, service de radiologie, Hôpital Rangueil, CHU de Toulouse, Toulouse
- Philippe Peti, PU-PH, chef de service, service d'imagerie pédiatrique et prénatale, Hôpital de la Timone Enfant, AP-HM, Marseille
- Pierre Potteche, CCA, département de radiologie diagnostique et thérapeutique, Hôpital François Mitterrand, CHU de Dijon, Dijon
- Alain Prigen, PU-PH honoraire, Université Paris Sud, Université Paris Saclay, Hôpitaux Universitaires Paris Sud
- Caroline Rousseau, MCU-PH, médecine nucléaire, ICO Gauducheau, Saint-Herblain
- Fabien Schneider, MCU-PH, radiologie centrale, Hôpital Nord, CHU de Saint-Étienne, Saint-Étienne
- Patrice Taoure, PU-PH, département d'imagerie médicale, Hôpital Lapeyronie, Université Montpellier 1, Montpellier
- Jean-Pierre Tasu, PU-PH, chef de service, service de radiologie, CHU de Poitiers, Poitiers
- Pierre Vera, PU-PH, directeur général, département radiologie et médecine nucléaire, QuantIF-Litis (EA4108 – FR CNRS 3638) CLCC Henri Becquerel, Rouen
- Paul Michael Walke, MCU-PH, imagerie médicale application clinique, département Vision, LE2I, UMR CNRS 6306, Faculté de médecine, Université de Bourgogne-Franche-Comté, Dijon
 |
Chapitre suivant |
 |
Retour au sommaire |
